GEODBONE: Una partícula para regeneración Ósea
Ventajas
- Dado su particular diseño, las superficies porosas, curvas, cóncavo/convexas de las partículas, aceleran la reproducción celular de los elementos que se depositen sobre ellas, facilitando la neoformación y favoreciendo la regeneración ósea del defecto en las que se han injertado.
- Dentro de un defecto óseo, las partículas en su conjunto cumplen una función de andamiaje con amplios espacios de formas aleatorias pero de paredes curvas, que permiten y facilitan el avance de vasos de neoformación entre las partículas, desde las paredes del defecto óseo hacia el centro del relleno; esto impide la formación de centros necróticos con partículas sin
vitalidad en el interior del injerto, problema que sí ocurre con injertos de partículas que quedan muy compactadas. - Dada su forma y su superficie porosa, cuando las partículas se depositan en un lecho óseo, se traban ente sí, permitiendo generar estructuras estables que rellenan el defecto más allá de los bordes iniciales, ganando en altura 1 o 2 mm, que en muchas ocasiones son fundamentales para la rehabilitación sobre implantes dentales de titanio.
Descripción
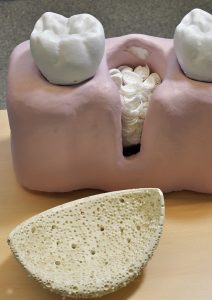 Biomaterial revolucionario con un diseño geométrico innovador en el área de los injertos óseos, que mejora el pronóstico de la regeneración ósea, especialmente en heridas de grandes volúmenes. La partícula que lo constituye, tiene un diseño específico y un método de fabricación particular, patentados, para regeneración ósea. Se ha diseñado y generado por prototipado rápido, con impresión 3D, una partícula con una forma específica que, al insertarlas en un defecto óseo, en conjunto promueven la regeneración celular y la reparación ósea, hacia el interior del injerto y permiten su crecimiento en altura.Diseño de injertos biológicamente activos, serviría como una nueva alternativa para el tratamiento de defectos óseos.Diseño de injertos biológicamente activos, serviría como una nueva alternativa para el tratamiento de defectos óseos
Biomaterial revolucionario con un diseño geométrico innovador en el área de los injertos óseos, que mejora el pronóstico de la regeneración ósea, especialmente en heridas de grandes volúmenes. La partícula que lo constituye, tiene un diseño específico y un método de fabricación particular, patentados, para regeneración ósea. Se ha diseñado y generado por prototipado rápido, con impresión 3D, una partícula con una forma específica que, al insertarlas en un defecto óseo, en conjunto promueven la regeneración celular y la reparación ósea, hacia el interior del injerto y permiten su crecimiento en altura.Diseño de injertos biológicamente activos, serviría como una nueva alternativa para el tratamiento de defectos óseos.Diseño de injertos biológicamente activos, serviría como una nueva alternativa para el tratamiento de defectos óseos
Diseño de injertos biológicamente activos, serviría como una nueva alternativa para el tratamiento de defectos óseos.
Mercado
El mercado está conformado por tres áreas:
- Área dental: Maxilofacial e implantología oral
- Área traumatológica: Traumatología de columna y cirugía ortopédica
- Área veterinaria: Cirugía ortopédica, especialmente caballar y vacuno (fina sangre y reproductores)
Se han identificado early adopters entre los dentistas implantólogos y los cirujanos de columna. No se ha investigado el mercado veterinario, pero parece interesante, al no poseer mayores normativas ni restricciones para su uso clínico.
Estado de desarrollo
- Se realizaron pruebas en rata (protocolo preestablecido en calota), con resultados satisfactorios.
- Se optimizaron las propiedades biomecánicas de la partícula
- Se están haciendo estudios comparativos con otras partículas de la competencia y con tejido óseo de diferentes zonas
Se están iniciando pruebas in vitro en animales grandes, en defectos de tamaño crítico, para demostrar su comportamiento en defectos de gran tamaño. - Se ha investigado el mercado nacional, a través de la metodología i-Corps. Se identificaron early adopters.
Aplicaciones
- Relleno de cavidades óseas post exodoncia
- Relleno de cavidades óseas dejadas por un quiste o un tumor extraído de la mandíbula, elevación del piso del seno maxilar, relleno de un defecto postquirúrgico en un hueso largo de una extremidad, etc.
- Aumento de la altura de una zona atrofiada de la mandíbula o de cualquier hueso del organismo (Nota: Habrá que tallar un lecho receptor que estabilice las primeras capas de partículas).
- Relleno óseo en una cirugía de fijación lumbar (artrodesis lumbar).
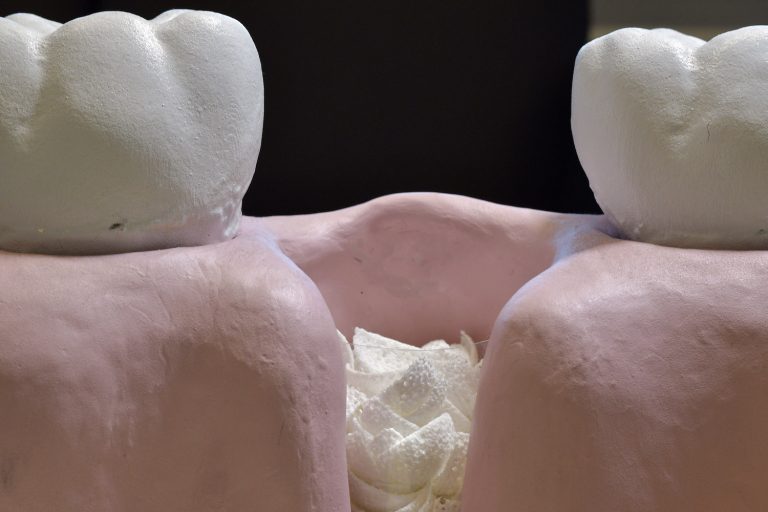
Su particular diseño curvo y poroso facilitaría la neoformación y favoreciendo la regeneración ósea del defecto en las que se han injertado.
Oportunidad
No existe un biomaterial para relleno de defectos óseos ideal, que cumpla todos los requerimientos clínico-quirúrgicos.
Los injertos actuales de índole biológico, derivados de hueso humano o animal, liofilizado, presentan riesgos de infección y/o rechazo; por su parte, los de índole sintético, tienden a infectarse y no integrarse con el hueso del lecho receptor.
En el mejor de los casos, si no se complican, demoran varios meses en integrarse al hueso circundante.
Reconocimiento del proyecto
Se ha investigado el mercado nacional, a través de la metodología i-Corps. Se identificaron early adopters.
Investigadores
 Alex Vargas D.
Alex Vargas D.
Odontólogo, Cirujano Maxilofacial
Departamento de Cirugía Oncológica y Maxilofacial
Facultad de Medicina
Pontificia Universidad Católica de Chile

Jorge Ramos G.
Ingeniero Civil Mecánico
Facultad de Ingeniería
Pontificia Universidad Católica de Chile
 Tomás Egaña
Tomás Egaña
Dr. Biología Humana – Universidad de Lübeck
Dr. Farmacología – Universidad de Chile
Profesor Asistente
Profesor Instituto de Ingeniería Biológica y Médica Pontificia Universidad Católica de Chile
Leave a reply
